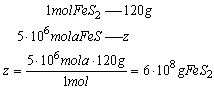W procesie spalania pirytu w fabryce kwasu siarkowego otrzymano 2*105...
W procesie spalania pirytu w fabryce kwasu siarkowego otrzymano 2*105m3 dwutlenku siarki w przeliczeniu na warunki normalne. Wydajność procentowa reakcji wynosiła 89,2%. Ile pirytu użyto do spalenia?
Rozwiązanie wybranego zadania z chemii
Wskazówka: Objętość dwutlenku siarki zamienimy na liczbę moli:
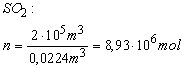
Na podstawie proporcji obliczymy ile moli siarki powstałoby, gdyby wydajność wynosiła 100%
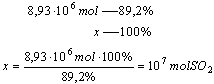
Zapiszemy równanie reakcji, ułożymy proporcje i obliczymy, ile zużyto pirytu:
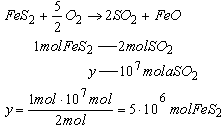
Masa jednego mola pirytu wynosi 120g. Ułożymy proporcję i obliczymy szukana masę pirytu: